امروزه تکنیکهای تکثیر و شناسایی اسیدهای نوکلئیک از مهمترین ابزارهای پژوهشهای زیستی و ژنتیکی به شمار میآیند. دانشمندان در همه زمینههای علوم زیستی، بیوتکنولوژی، پزشکی، پزشکی قانونی، تشخیصی و … از این روشها در طیف گستردهای از کاربردها استفاده میکنند. برای برخی از کاربردها، تشخیص کیفی اسید نوکلئیک کافی است. در حالی که تحقیقات در سایر زمینهها نیاز به تجزیه و تحلیل کمی دارند. Real – Time PCR میتواند برای تجزیه و تحلیل کمی و کیفی اسیدهای نوکلئیک مورد استفاده قرار گیرد.
در این مطلب به بررسی روش Real – Time PCR، تکنیکهای کمی PCR با رونویسی معکوس و معرفی ابزارهایی که تاکنون برای این تکنیکها ارائه شده، میپردازیم. همچنین راهنماییهایی درباره مراحل جداسازی RNA مانند جمع آوری نمونه، استخراج RNA و تجزیه و تحلیل کیفیت و کمیت RNA ارائه میکنیم.
PCR در زمان واقعی چیست؟
در PCR معمولی، محصول DNA تکثیر شده یا آمپلیکون در یک تحلیل نقطه انتهایی شناسایی میشود. در حالی که PCR در زمان واقعی، تجمع محصول ایجاد شده را در طی روند پیشرفت واکنش PCR به طور همزمان نشان میدهد به طوری که کمیت محصول پس از هر بار انجام چرخه PCR اندازهگیری میشود.
مراحل انجام PCR در زمان واقعی در شکل زیر مشخص شده است. در اولین مرحله، اجزای واکنشهای PCR رشتههای هدف به همراه پرایمرهای اختصاصی آماده میشوند. سپس اجزای واکنش PCR با توجه به پروتکل مشخص، در لولههای واکنش با هم ترکیب میشوند و لولهها درون دستگاه PCR در زمان واقعی قرار میگیرند. پس از تنظیم دستگاه، واکنش PCR شروع میشود. همزمان با شروع چرخههای PCR دادههای جمع آوری شده توسط نرم افزار یا ابزار اختصاصی دستگاه مورد تجزیه و تحلیل قرار میگیرند.

تشخیص به وسیله تکنیک PCR در زمان واقعی، با اضافه کردن یک مولکول فلورسنت به عنوان گزارشگر به محصولات PCR در هر لوله واکنش انجام میگیرد، به طوری که با پیشرفت واکنش و افزایش مقدار DNA تولید شده در هر چرخه، فلورسانس ایجاد شده به وسیله مولکول گزارشگر نیز افزایش مییابد که این افزایش با حسگرهای دستگاه قابل شناسایی است.
مواد شیمیایی فلورسانس به کار رفته برای این منظور شامل رنگهای متصل شونده به DNA و توالیهای پرایمر یا پروب نشان دار شده با فلورسانس هستند. برای ردیابی و نظارت بر سیگنال فلورسانس این پروبهای نشان دار شده، دستگاههای ترموسایکلر تخصصی مجهز به حسگرهای تشخیص فلورسانس همزمان با پیشرفت چرخههای PCR و تولید محصولات آنها، طراحی شده است. فلورسانس اندازهگیری شده متناسب با مقدار کل آمپلیکون یا DNA تکثیر شده است. تغییر فلورسانس به مرور زمان برای محاسبه مقدار آمپلیکون تولید شده در هر چرخه مورد استفاده قرار میگیرد.
مهمترین مزیت PCR در زمان واقعی نسبت به PCR معمولی این است که PCR در زمان واقعی به شما امکان میدهد، تعداد اولیه نسخههای DNA الگو (توالی هدف) را با دقت و حساسیت بالا در روند انجام چرخههای واکنش تعیین کنید.
نتایج PCR در زمان واقعی میتواند کیفی (تعیین حضور یا عدم وجود یک توالی) یا کمی (تعیین تعداد نسخههای توالی هدف) باشد. PCR در زمان واقعی کمی، نیز به عنوان روش qPCR یا Quantitative real-time PCR شناخته میشود.
PCR معمولی در بهترین حالت میتواند نتایج واکنشها را به صورت کیفی (با استفاده از تکنیک ژل الکتروفورز) ارائه دهد. علاوه بر این، دادههای PCR در زمان واقعی بدون نیاز به انجام ژل الکتروفورز قابل ارزیابی هستند، به همین دلیل با PCR در زمان واقعی، در زمان و هزینههای انجام واکنش صرفه جویی میشود. در نهایت، از آن جایی که واکنشهای این نوع از تکنیک PCR، همزمان با پیشرفت واکنشها قابل ردیابی هستند؛ دادهها در یک سیستم qPCR یکپارچه، با لوله بسته (بدون نیاز به دستکاری واکنشها) ارزیابی میشوند و به این ترتیب امکان ایجاد آلودگی در واکنشها کاهش مییابد و نیاز به دستکاریهای بعد از تکثیر یا Postamplification در تجزیه و تحلیل qPCR وجود ندارد.
کاربردهای آزمون PCR / qPCR در زمان واقعی
آزمون PCR /qPCR در زمان واقعی به ابزار انتخابی جهت شناسایی سریع، حساس و اختصاصی رشتههای اسیدهای نوکلئیک است و همچنین میتواند مقادیر کمی اسیدهای نوکلئیک را در نمونههای مختلف بیولوژیکی مشخص کند.
تکنیک Real-time PCR در برنامههای کاربردی متنوعی همچون تجزیه و تحلیل بیان ژن، تشخیص و شناسایی ارگانیسمهای اصلاح شده ژنتیکی در مواد غذایی و ژنهای دخیل در سرطان مورد استفاده قرار میگیرد.
در آزمایشگاههای تحقیقاتی، واکنشهای qPCR به طور گسترده برای اندازه گیری کمی تعداد کپیهای ژن یا به اصطلاح دوز ژن در ردههای سلولی مختلف و یا حضور ژنهای جهش یافته در نمونه مورد استفاده قرار میگیرند. چنانچه تکنیک Real-time PCR در کنار روش PCR با رونویسی معکوس (RT-PCR) انجام شود، از این تکنیکها میتوان برای اندازهگیری دقیق تغییرات در بیان ژن استفاده کرد. به عنوان مثال، افزایش یا کاهش بیان یک ژن در پاسخ به شرایط مختلف محیطی یا درمان دارویی، با اندازهگیری تغییرات mRNA. در سطح سلولی قابل اندازهگیری است.
کاربردهای این تکنیک را به اختصار میتوان به صورت زیر بیان کرد:
- بررسی بیان ژن
- اندازهگیری میزان همانند سازی DNA در ژنوم
- بررسی بیان ژن در اثر داروها
- تشخیص جهشهای DNA
- شناسایی پاتوژنها
- تعیین ژنوتیپ افراد
PCR در زمان واقعی چگونه کار می کند؟
برای درک چگونگی عملکرد PCR در زمان واقعی، یک نمودار از تجزیه و تحلیل دادههای PCR در زمان واقعی را در شکل زیر ارائه کردهایم. در این نمودار، تعداد چرخه PCR در محور x نشان داده شده است و شدت فلورسانس حاصل از واکنشهای چرخه PCR که متناسب با مقدار محصول تکثیر شده در لولههای واکنش است، در محور y نمایش داده شده است.
این نمودار، تکثیر توالیها در دو مرحله را نشان میدهد. یک مرحله نمایی یا تصاعدی است و به دنبال آن مرحله دوم یک روند غیر نمایی را به نمایش میگذارد. در طول مرحله نمایی، مقدار محصول PCR در هر چرخه تقریباً دو برابر میشود. با ادامه چرخههای واکنش، به دلیل این که اجزای واکنش در طول پیشرفت چرخهها مصرف میشوند و در نهایت تعداد محدودی از آنها برای ادامه انجام چرخهها باقی میمانند که باعث کاهش سرعت تولید محصولات PCR میشوند. در این مرحله، واکنش کند شده و وارد مرحله پایا میشود (در محدوده چرخه های 28 تا 40).
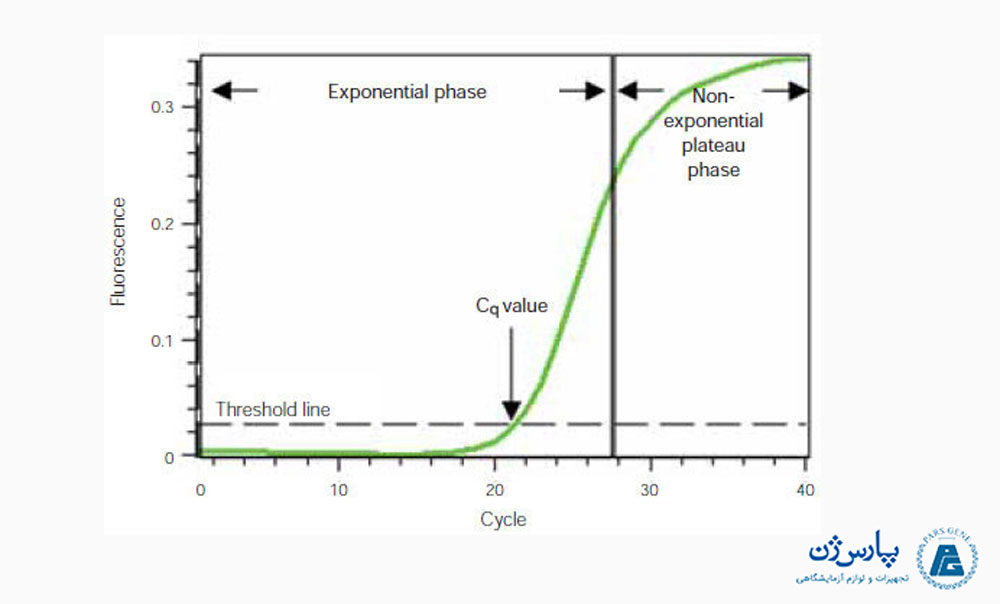
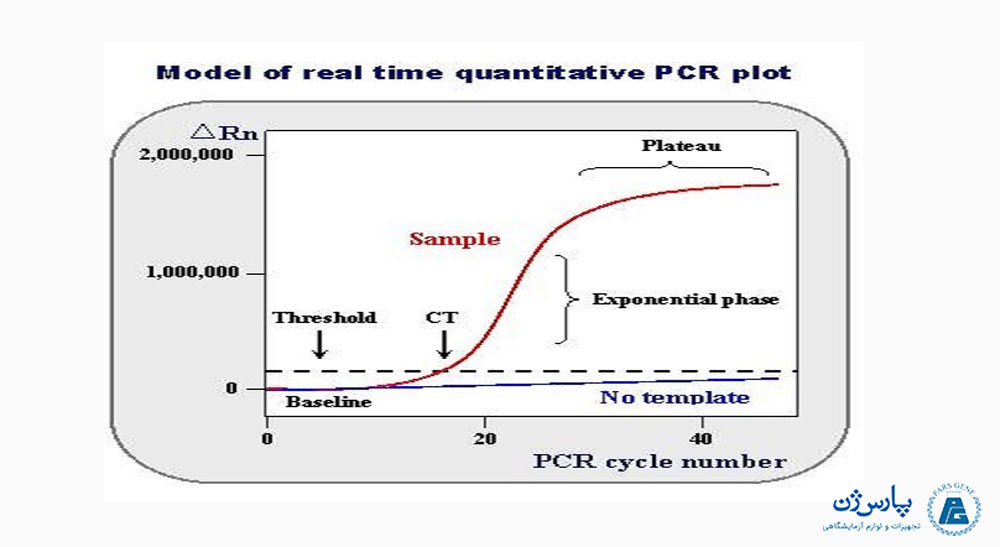
در شروع واکنشهای PCR، فلورسانس در سطح پس زمینه (پایین نمودار) باقی میماند و افزایش در فلورسانس قابل ردیابی نیست (چرخه 1-18، شکل 1) زیرا میزان محصولات به اندازهای نیست که فلورسانس منتشر شده از آنها توسط حسگرهای دستگاه مشاهده شود. با ادامه چرخههای واکنش، محصول تکثیر شده به اندازه کافی در لولههای واکنش تجمع پیدا میکند تا سیگنال فلورسانس قابل ردیابی توسط دستگاه را به دست آورد. شماره چرخهای که اولین سیگنال فلورسانس از آن ردیابی میشود، حد آستانه یا Ct (Cycle Of Threshold) نامیده میشود. از آنجا که مقدار Ct در مرحله نمایی نمودار اندازهگیری میشود یعنی زمانی که اجزای واکنش محدود نیستند، میتوان از qPCR در زمان واقعی برای محاسبه قابل اطمینان و دقیق مقدار اولیه توالی هدف یا الگوی موجود در واکنش استفاده کرد. این محاسبه براساس عملکرد شناخته شده نمایی پیشرفت واکنش قابل انجام است.
حد آستانه یا Ct یک واکنش عمدتا با مقدار الگوی موجود در شروع واکنش PCR تعیین میشود. اگر مقدار زیادی از الگوی در شروع واکنش وجود داشته باشد، تعداد چرخه PCR تقریباً کمی لازم خواهد بود تا محصول کافی برای ارائه سیگنال فلورسانس در پس زمینه ردیابی شود. بنابراین، واکنش PCR، Ct کم یا زودهنگام خواهد داشت. در مقابل، اگر مقدار کمی از توالی الگوی در شروع واکنش وجود داشته باشد، برای افزایش سیگنال فلورسانس نیاز به انجام چرخههای PCR بیشتری است تا مقدار سیگنالهای فلورسانس به حد اندازهگیری برسد. بنابراین، Ct واکنش بالا یا دیررس خواهد داشت. این رابطه پایهای برای اندازهگیریهای کمی PCR در زمان واقعی است.
مراحل انجام تکنیک Real-Time PCR
مراحلی که باید برای انجام یک واکنش PCR در زمان واقعی انجام شود، مشابه مراحل واکنش PCR معمولی است با این تفاوت که در Real-Time PCR برای تولید فلورسانس جهت شناسایی و تعیین میزان محصولات تولید شده در هر چرخه باید از پرایمرها یا پروبهای گزارشگر یا فلوئوفورها استفاده کرد. بر این اساس مراحل انجام Real-Time PCR به صورت زیر است:
مرحله پایه:
در این مرحله مقدار محصولات تولید شده در چرخهها کمتر از حد آستانه است و بر روی نمودار شدت فلورسانس قابل مشاهده نیست.
مرحله نمایی:
با شروع مرحله رشد تصاعدی در هر چرخه، مقدار محصولات دو برابر میشود و در نمودار، رشد نمایی مربوط به واکنش نشان داده میشود..
مرحله خطی:
زمانی که ترکیبات واکنش بسیار محدود میشوند.
مرحله ایستا:
در این مرحله به دلیل اتمام و محدود شدن اجزای اولیه واکنش، شدت فلورسانس تغییر نمیکند.
استفاده از رنگ های فلورسنت به عنوان مولکول گزارشگر
در واکنشهای تکنیکReal timePCR ، اغلب میتوان از دو نوع رنگ فلورسنت به عنوان مولکول گزارشگر استفاده کرد:
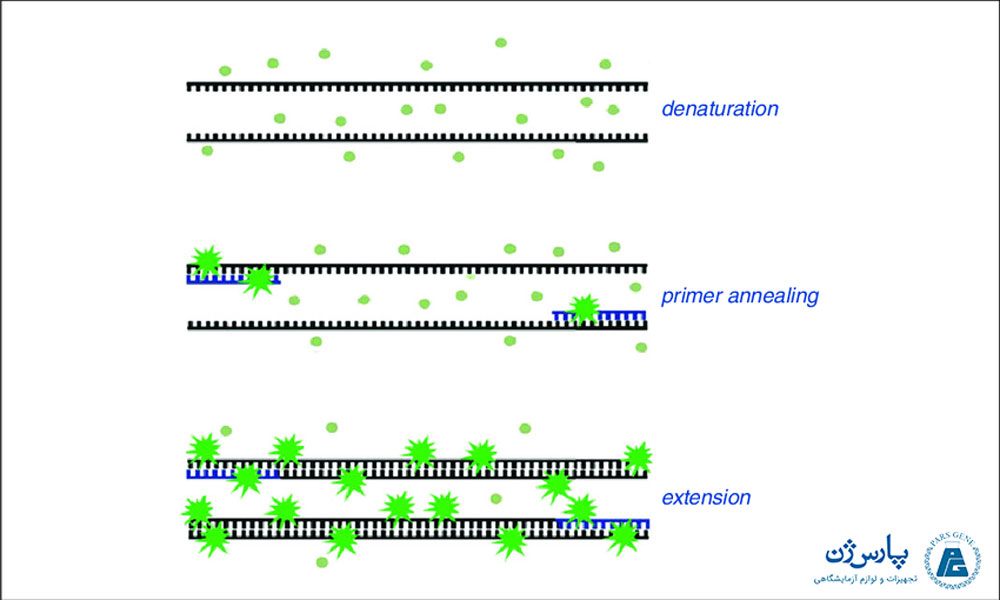
سایبر گرین:
متداولترین رنگ فلورسنت سایبرگرینSYBR Green)) است که در اغلب آزمایشگاهها از این رنگ استفاده میشود. مکانیسم عمل سایبرگرین به این صورت است که فقط میتواند به شیارهای کوچکDNA دورشتهای متصل شود و با جذب طول موج 498 نانومتر، نور را در ۵۲۲ نانومتر منتشر میکند. این نور برای حسگرهای دستگاه Real-Time PCR قابل ردیابی و اندازهگیری است. سایبر گرین به دلیل این که میتواند به تمام توالیهای دو رشتهای متصل شود به صورت غیر اختصاصی عمل میکند؛ اما از آن جایی که کاربردی آسان، قیمت ارزان و سمیت کمی دارد به طور معمول در اکثر واکنشهای Real-Time PCR مورد استفاده قرار میگیرد.
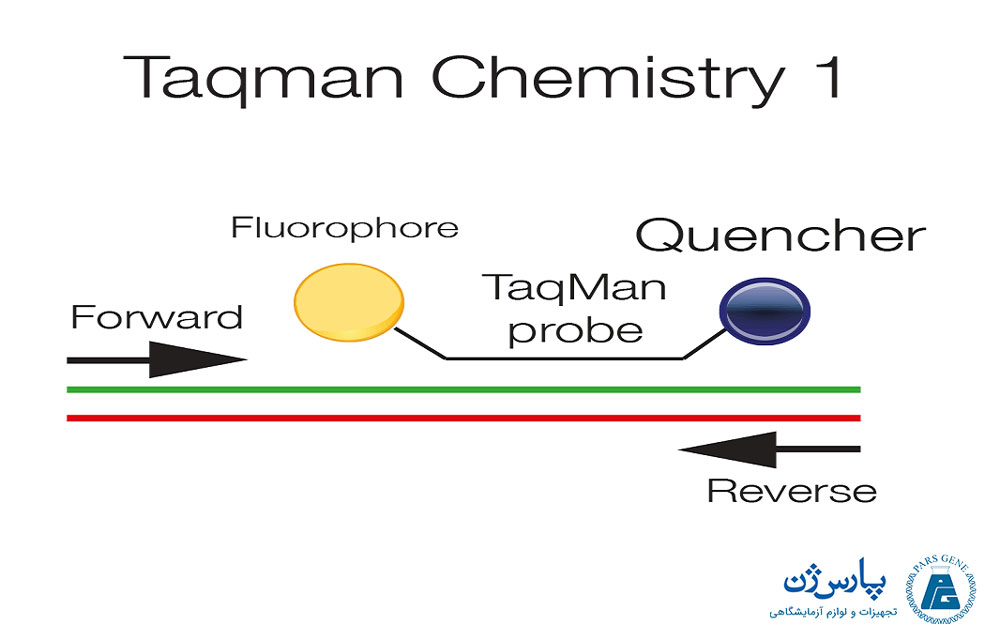
پروبهای نشان دار:
این پروبها، توالیهای الیگونوکلوئيدی نشان داری هستند که به طور اختصاصی برای هر توالی هدف ساخته میشوند. بنابراین استفاده از پروبها، موجب افزایش دقت و اختصاصیت واکنشهای Real-Time PCR میشود. از معمولترین پروبهایی که در این واکنشها به کار میروند، میتوان به پروب Taq Man اشاره کرد. مکانیسم عمل این پروبها به این صورت است که در یک سر خود دارای رنگ فلورسنت یا فلوئوفور (Reporter) و در سر دیگر توالی این پروبها مولکولهای خاموش کننده یا (Quencher) قرار دارند و زمانی که پروب به توالی تک رشتهای هدف متصل است، مولکول گزارشگر به حالت خاموش قرار دارد و با شروع چرخههای واکنش و ساخت توالیهای دو رشتهای مولکول فلوئوفور از خاموش کننده جدا شده و نور منتشر میکند که توسط دستگاه قابل ردیابی است.
جداسازی RNA
جمع آوری نمونه
برای جداسازی RNA و تعیین میزان بیان ژن، مواد نمونه باید تا حد ممکن یکدست باشند. اگر نمونه بافتی شما شامل بسیاری از انواع مختلف سلول است، نشان دادن الگوی بیان ژن مورد نظر ممکن است مشکل باشد. اگر نمونه ناهمگنی دارید، از یکی از روشهای متعددی که برای جداسازی و تخلیص انواع سلولهای خاص در دسترس است، استفاده کنید. از جمله این روشها میتوان به کالبد شکافی بافت، بیوپسی یا تکه برداری با سوزن و نمونه برداری با لیزر اشاره کرد. سلولهای جمع آوری شده سپس میتوانند برای استخراج نمونههای RNA مورد استفاده قرار گیرند.
استخراج RNA
RNA كل یا پلی RNA (A +) میتواند برای بیشتر کاربردهای RT-qPCR در زمان واقعی مورد استفاده قرار گیرد. یک نکته مهم در کار با RNA، از بین بردن آنزیمهای RNases در محلولها، مواد مصرفی و سطوح کار در آزمایشگاه است. برای این کار میتوان از محلولهای آماده موجود در بازار که بدون RNase یا RNase free هستند، استفاده کرد یا محلولهایی که در آزمایشگاه تهیه میکنید را با دی اتیل پیروکربنات (DEPC) تیمار و سپس اتوکلاو کنید. RNases موجود در وسایل آزمایشگاهی را همچنین میتوان با استفاده از روش DEPC یا با حرارت دادن در 250 درجه سانتیگراد به مدت 3 ساعت غیرفعال کرد.
نمونههای RNA آماده ممکن است گاهی لازم باشد برای جلوگیری از تکثیر احتمالی هر گونه DNA ژنومی آلوده، با DNase مورد تیمار قرار گیرند. در صورتی که نمونهها قبل از انجام PCR از آلودگیهای DNA ژنومی پاکسازی نشوند، ممکن است در نتایج واکنشها تعدادی بیش از مقدار واقعی کپیهای mRNA را نشان دهند. با این حال، هنگامی که نمونه اولیه برای شروع واکنش PCR محدود است، ممکن است نتوان از DNase استفاده کرد، زیرا دستکاری اضافی محلولهای واکنش میتواند باعث از دست رفتن نمونههای RNA شود.
تجزیه و تحلیل کمی و کیفیت اسید نوکلئیک
اندازه گیری دقیق اسید نوکلئیک اسید برای تجزیه و تحلیل بیان ژن ضروری است؛ به ویژه هنگامی که مقدار RNA کل برای نرمال سازی بیان ژن هدف مورد استفاده قرار میگیرند. غلظت و خلوص RNA معمولاً با اندازهگیری نسبت جذب اشعه ماوراء بنفش در 260 نانومتر و 280 نانومتر تعیین میشود.
PCR رونویسی معکوس کمی (RT-qPCR)
دو روش برای تعیین کمیت بیان ژن توسط RT-qPCR در دسترس است:
- RT-qPCR دو مرحلهای
- RT-qPCR یک مرحلهای
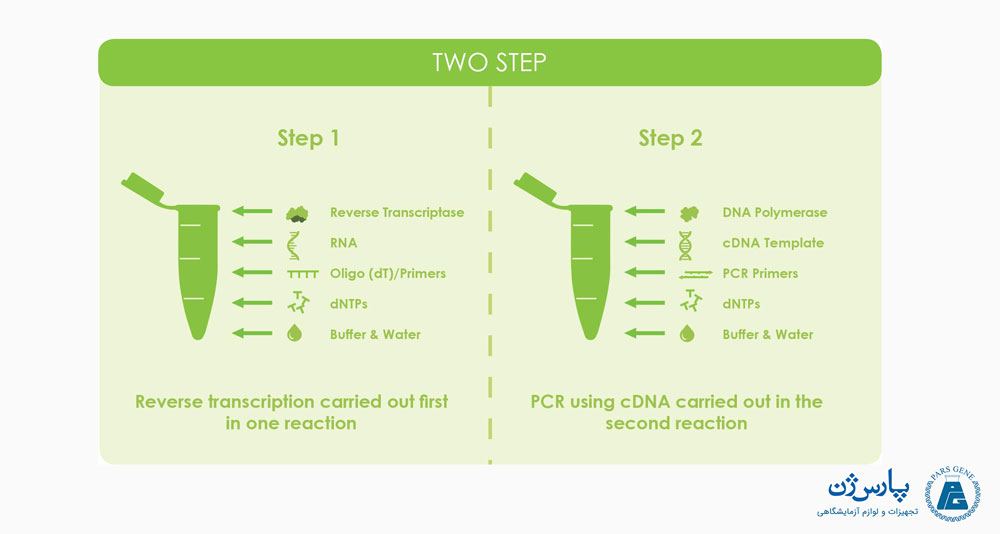
در هر دو مورد روش، آنزیم رونوشت بردار معکوس RNA را به cDNA رونویسی میکند و از این cDNA به عنوان الگوی تکثیر در واکنشهای qPCR استفاده میشود. دو روش تک مرحلهای و دو مرحلهای با توجه به این که آیا PCR رونویسی معکوس کمی و واکنش تکثیر PCR در زمان واقعی در لولههای یکسان یا جداگانه انجام میشود، از هم متمایز میشوند.
روش دو مرحلهای
در روش دو مرحلهای، ابتدا RNA در واکنش با استفاده از آنزیم رونوشت بردار معکوس به cDNA رونویسی میشود. سپس cDNA حاصل، به عنوان یک توالی الگو برای واکنشهای qPCR چندگانه، به مصرف میرسد.
روش یک مرحلهای
در روش یک مرحلهای، دو واکنش PCR رونویسی معکوس کمی و qPCR در زمان واقعی در یک لوله واکنش انجام میگیرند.
دستگاههای qPCR / Real PCR
یک سیستم تشخیصی PCR در زمان واقعی، شامل یک چرخه حرارتی مجهز به یک حسگر تشخیص نوری برای اندازهگیری سیگنالهای فلورسانس تولید شده در هر چرخه تکثیر است. سیگنالهای فلورسانس از فلوروفورهای متصل به پرایمرها یا پروبهایی که به توالی هدف اتصال مییابند، منتشر میشوند. شکل ۹: دستگاه Real – Time PCR


